Dalam ilmu kimia dasar, kita akan menjumpai empat istilah yakni isotop, isobar, isoton, Isoelektron. Apa itu? Apa maknanya? dan Seperti apa contohnya?. Nah, dalam postingan ini kamu akan mengetahui keempat istilah tersebut beserta contoh dan fungsinya.
Kali ini, kamu akan mengetahui tentang isotop, isobar, isoton, dan isoelektron yang merupakan pembahasan dasar dalam ilmu kimia yang masuk dalam topik struktur atom.
Isotop adalah
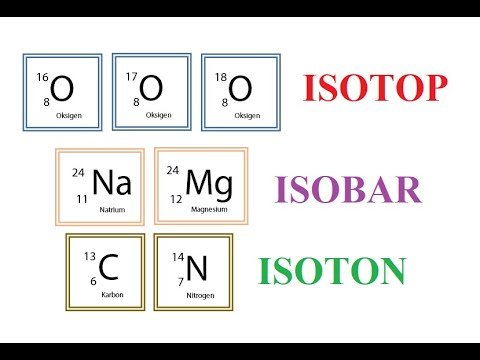
Atom-atom yang mempunyai nomor atom yang sama tetapi berbeda nomor massanya disebut isotop (isotope). Sebagai contoh, terdapat tiga isotop untuk hidrogen.
Penemuan isotop pertama adalah pada hidrogen yang mempunyai satu proton dan tidak mempunyai neutron. Isotop deuterium mempunyai satu proton dan satu neutron, dan tritium mempunyai satu proton dan dua neutron.
Perhatikanlah contoh isotop-isotop atom hidrogen berikut ini!

Sifat-sifat kimia suatu unsur terlihat terutama pada proton dan elektron dalam atomnya.
Namun neutron tidak ikut serta dalam perubahan kimia pada keadaan normal.
Isotop-isotop dari unsur yang sama mempunyai sifat-sifat kimia yang sama, membentuk jenis senyawa yang sama, dan menunjukkan kereaktifan yang serupa.
Isobar adalah
Isobar adalah atom dari unsur yang berbeda (mempunyai nomor atom berbeda) tetapi mempunyai jumlah nomor massa yang sama.
Isoton adalah
Isoton adalah atom dari unsur yang berbeda (mempunyai nomor atom dan nomor massa berbeda), tetapi mempunyai jumlah neutron yang sama.
Isoelektron adalah
Untuk memahami pengertian isoelektron coba perhatikan contoh isoelektron berikut ini!
- 9F– dan 8O2- mempunyai 10e-
- 7N3- dan 8O2- mempunyai 10e-
- 9F– dan 10Ne mempunya 10e-
Berdasarkan contoh di atas terlihat 9F–, 7N3-, O2- dan Ne mempunyai 10 elektron.
Jadi: Ion-ion dan unsur (9F–, 7N3-, O2- dan Ne) tersebut adalah isoelektron.
Karena memiliki jumlah elektron sama, yaitu 10 elektron.
Sehingga juga memiliki konfigurasi elektron yang sama, yaitu 1s2 2s2 2p6.
Berdasarkan uraian di atas dapat disimpulkan
Bahwa isoelektron adalah unsur atau ion yang mempunyai jumlah elektron sama, untuk lebih memahaminya perhatikan !
Baca Juga:
Untuk mencapai kestabilan seperti konfigurasi elektron gas mulia, unsur golongan 1A (1) dan 2A (2) cenderung untuk melepaskan elektron valensinya sehingga membentuk ion positif (kation).
Sedangkan unsur golongan 6A (16) dan 7A (17) cendrung membentuk ion negatif (anion). Ion-ion ini dikatakan isoelektronik (iso Yunani, “sama”) dengan gas mulia terdekat.
Gambar menunjukkan hubungan ini.
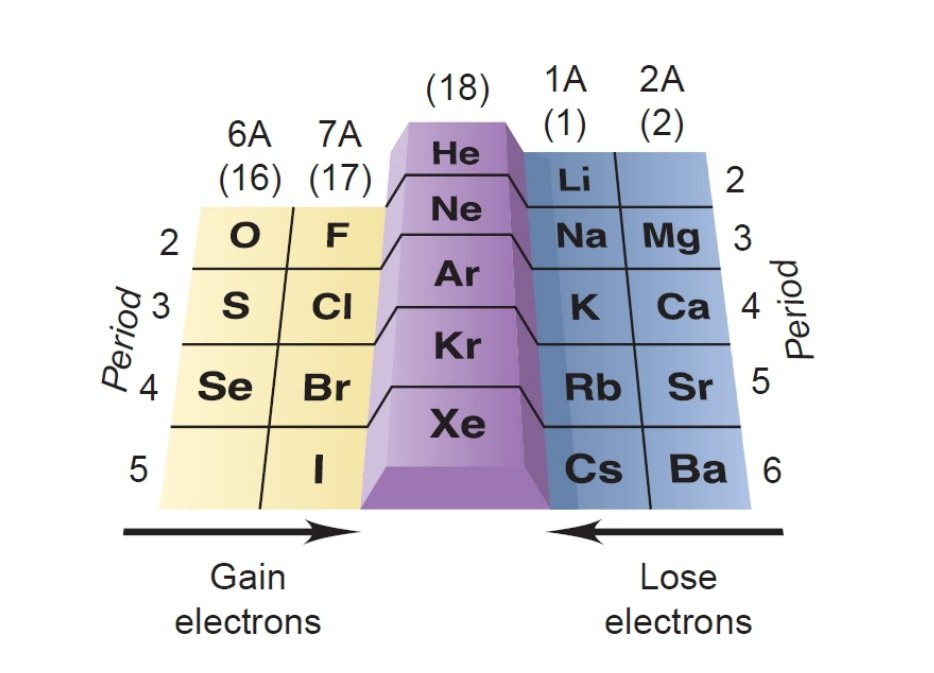
Ketika atom logam alkali [Grup 1A (1)] kehilangan elektron valensi tunggalnya, ia menjadi isoelektronik dengan gas mulia sebelumnya.
Sebagai contoh ion Na+ (1s22s22p6) isoelektronik dengan neon (Ne):
Ne (1s2 2s2 2p6).
Ketika atom halogen [Grup 7A (17)] menerima satu elektron, maka ia menjadi isoelektronik dengan gas mulia berikutnya.
Contoh:
Ion bromida isoelektronik dengan krypton
(Kr): Br ([Ar] 4s2 3d10 4p5),
Br ([Ar] 4s2 3d10 4p6) [isoelektronik dengan Kr ([Ar] 4s2 3d10 4p6)].
Sebagian besar unsur yang membentuk ion monatomik yang isoelektronik dengan gas mulia terletak pada empat kelompok yang mengapit golongan 8A (18), dua di kedua sisi.
Akhir Kata
- Isotop adalah atom-atom yang mempunyai nomor atom yang sama tetapi berbeda nomor massanya.
- Isobar adalah atom yang mempunyai nomor atom berbeda tetapi mempunyai nomor massa yang sama.
- Isoton adalah atom yang mempunyai nomor atom dan nomor massa berbeda tetapi mempunyai jumlah neutron yang sama.
- Isoelektron adalah atom atau ion yang memiliki jumlah elektron yang sama, sehingga konfigurasi elektronnya juga sama.



![Download Modul Ajar Matematika Kelas 1 Semester 1 dan 2 Kurikulum Merdeka [gurusekali]](https://jalanguru.com/wp-content/uploads/2023/01/Download-Modul-Ajar-Matematika-Kelas-1-Semester-1-dan-2-Kurikulum-Merdeka-gurusekali-e1759648826168-150x150.jpg)








